【医学】再生医学材料-商业化
近日,美国 加利福尼亚大学尔湾分校(University of California,Irvine)Takumi Takahashi,Kyriacos A. Athanasiou等,在Nature Reviews Bioengineering上发表综述文章,讨论了商业化的关键方面,即保护知识产权、引导监管路径和获得资金,并重点介绍了成功开发美国食品和药物管理局批准再生药物产品的学术初创公司,以及因其正在开发的再生药物产品,而获得再生医学先进疗法称号公司的案例研究。

Commercialization of regenerative-medicine therapies.
再生医学疗法的商业化。
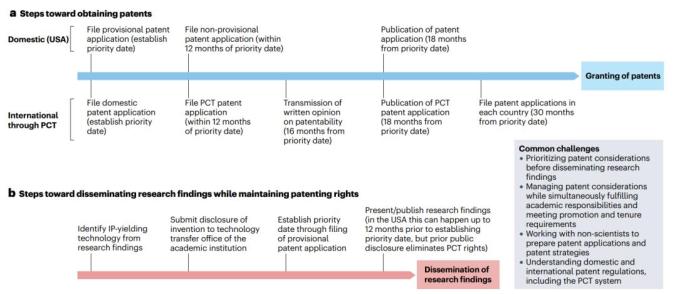
图1:在维护专利权的同时,获得专利和传播研究成果步骤。
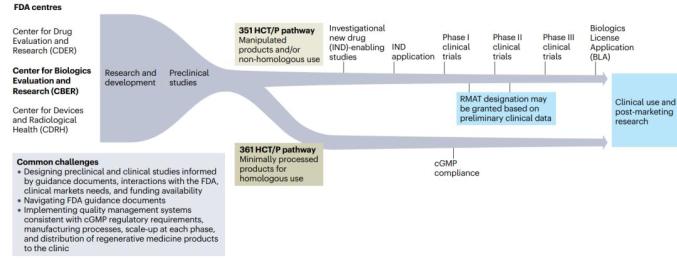
图2:针对再生药物疗法,美国食品和药物管理局Food and Drug Administration,FDA的监管途径。
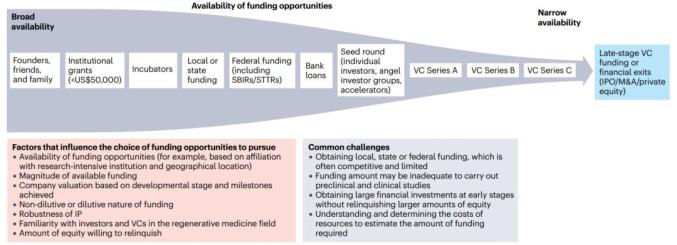
图3:学术创业的资助机制。
关键点
1、将再生药物疗法转化为批准产品感兴趣的学术研究人员,会受益于在研究和开发早期了解商业化方面的知识。
2、在学术机构内,了解建立知识产权 intellectual property (IP) 步骤是,开展和传播产生知识产权研究的关键所在。
3、再生医学先进疗法Regenerative Medicine Advanced Therapy (RMAT)的命名,提供了一种途径,可以加快再生医学产品的审批过程。
4、基金和非稀释non-dilutive发行机制,支持临床前研究,而资金和首次公开发行的稀释机制是临床开发阶段金融资本的主要来源。
5、学术机构和资助机构,应实施政策变革,以激励和推动学术研究人员将再生医学技术商业化。
文献链接
Takahashi, T., Donahue, R.P., Nordberg, R.C. et al. Commercialization of regenerative-medicine therapies. Nat Rev Bioeng (2023).
https://doi.org/10.1038/s44222-023-00095-9
https://www.nature.com/articles/s44222-023-00095-9
本文译自Nature。










































